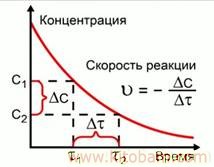
سورعت ریکسیة شیمیایی، مفهوم اساسی کینیتیکة شیمیاییست، که تغییر یافتن عدد ذرهها (مالیکولهها، یونها)-ا همه گونه مادّة در ریکتسیه اشتراککننده را در واحد وقت به واحد حجم (برای ریکتسیههای گاماگینی) یا به واحد مساحت سطح (برای ریکتسیههای گیتیراگینی و تاپاخیمیوی) افاده میکند. سرعت ریکسیههای شیمیایی را مقداراً از روی تغییر کانسینترتسیة مادّههای به ریکتسیه داخلشونده یا محصول ریکسیه مویین میکنند. مالیکولهها در واحد وقت هر قدر زیادتر به هم برخورند، سرعت ریکسیههای شیمیایی همان قدر زیاد میشود. هنگام بلند شدن حرارت سرعت حرکت مالیکولهها زیاد شده، سبب افزودن عدد مالیکولههای به هم برخورنده میگردد. برابر این سرعت ریکسیههای شیمیایی زیاد میشود. هنگام بلند شدن حرارت به هر 10°س سرعت ریکسیههای شیمیایی گاماگینی متناسباً 2-4 مراتبه میافزاید (قانون ونت-گافّ). سرعت ریکسیههای شیمیایی را اینچنین با کتلیزتارها نیز تغییر دادن ممکن است. سرعت تبدّلات گوناگون شیمیایی در طبیعت هر خیل است. مثلاً، خادیسههای ترکش ورعد و برق (از ده هزار یک قسم ثانیه) ، حادثة زنگزنی متالها و مصنوعات متالی، به وجود آمدن مینیرلها و غیره دهها، صدها و هزارها سال دوام میکنند. حالا انسانیت شرایط بوجودایی ریکتسیههای شیمیایی را به حساب گرفته، سرعت آنها را در صناعت تغییر داده، برای ثمرهناکی محصولات شیمیایی، پیشرفت خواجگی خلق استفاده میبرند. سرعت ریکسیههای شیمیایی را با اصولهای فاتامیتر، پالیراگرفی، پاتینسیامیتری و غیره مویین میکنند.
دبیات: ایمنوال ن. م. ، کنارّی د. گ. کورس خیمیچیسکایی کینیتیک، مسکو، 1974؛ گلینکه ن. ل. ، آبشیه شیمی، لنینگراد. 1977. ن. قابلاو.
 Таджикистан – Энциклопедия на таджикском языке КИТОБАМ
Таджикистан – Энциклопедия на таджикском языке КИТОБАМ